-
应用笔记 · 2025年08月12日
应用笔记 | Opentrons Flex 驱动的全自动化样本制备,助力 TMT 标记多重 LC-MS 蛋白质组学分析
阅读全文 -
应用笔记 · 2025年07月14日
应用笔记 | 基于 Opentrons Flex 的自动化蛋白质酶解与纯化
阅读全文 -
应用笔记 · 2025年07月07日
应用笔记 | 基于 Opentrons Flex 的自动化蛋白质浓度定量与均一化处理
阅读全文


应用概述
随着不断进步的技术推动,现代分子生物学持续取得万众瞩目的 突破和发展,包括更大规模的研究、更强大的治疗方法以及全新 的研究问题。然而,尽管核酸提取这项技术是分子生物学得以进 步的一项重要且密不可分的实验环节,科研人员仍然在沿用着几 十年前冗长而繁琐的程序进行核酸提取。在这样的困局之下,自 动化解决方案应运而生。现代自动化通过引入具备稳定性和高效 运作优势的机器设备完成标准化流程高效自动运行,自动化核酸 提取将使生物实验室旧有的工作方式迎来现代化。为了真正意义 上帮助科研人员达到高效研发或生产的目的,自动化系统需要达 到甚至超越高技能技术人员的表现,为下游工作流程提供高质量的样本。
本项研究旨在测试Opentrons OT-2核酸工作站作为有效自动化 磁珠基因提取工具的性能。研究中使用了几种研究人员和临床医 生常用的常见模板:人类唾液、人类口腔拭子、细菌培养物和 RNA 病毒。同时,使用了行业中常见的主流试剂品牌。通过产 量、CV 值和qPCR 数据进行性能评估,实验数据将与高技能技术人员的手动操作结果进行比较。
经过研究测试,OT-2 表现优异。使用OT-2 进行提取的实验变异 性降低,同时复现率提高,并且能在较低的成本和更快的周转时 间下提供了类似的产量。重要的是,这些性能改进和成本节省可 以随着吞吐量的增加而提升。因此,该测试表明,使用 OT-2 进 行核酸提取自动化可以使实验流程高效自动化,让自动化核酸提取能够满足高端分子生物学的高性能标准。
研究材料和方法
人类唾液: 从匿名捐赠者处收集新鲜唾液并储存在15 mL 锥形管中直至使用。
口腔拭子:使用20 mm break point (Zymo@) 口腔采集拭子对匿名 志愿者进行采样,并储存于在1 mL Zymo DNA/RNA 保护液中,室温保存运输,
细菌培养: 使用 One shot°TOP10 制备感受态大肠杆菌 (Thermo Fisher Scientific*) 在37°℃,225 rpm 振荡条件下在溶菌液中培养过 夜。使用前,每个样品用2000 rpm 离心1.5 分钟。去除上清液,沉淀物被重新悬浮于等体积的冷磷酸盐缓冲液中。此外,对于乳酸杆菌样品,每个样品使用约1×107拷贝/μL的 Lactobacillus plantarum(ATCC°8014MINIPACKTM)。
病毒:由于2020年3月COVID-19 全球大流行开始(1),病毒 RNA 试剂盒中使用了的合成 SARS-COV-2 RNA Control 2(Twist Biosci- ences), 每个样品10拷贝/μL。
内部对照:按照 Panpradist、Nuttada 等人(2)中所述使用和创建合 成鼻样基质(SNM)。SNM 的配方为:110 mM NaCl、1%w/v来自猪 胃类型I的粘蛋白(Sigma M2378-100G)和10 μg/mL w/v 人类基 因组DNA(Coriell NA12878), 混合体积为TE/SNM的90%。每个病毒样本使用50 pg/μL的 SNM。
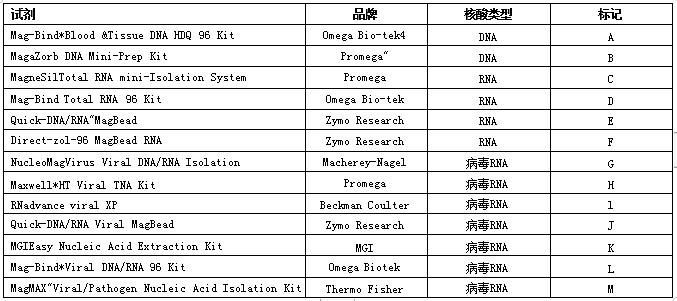
试剂盒:本项研究中选择了来自不同品牌的 DNA、RNA 和病毒 RNA提取试剂盒(参见表1)。总共检验了7个试剂品牌的13种试剂盒。
提取: 在自动化检测之前,我们对每个 DNA 和 RNA 提取试剂及 模板进行了手动测试,以获取手动测试基线浓度。每个模板在每 种试剂中进行7次重复测试,并配备1 个阴性对照样本。本次研 究在 Opentrons 平台上进行了自动化核酸提取。对于 DNA 和 RNA 提取试剂,每个样本进行了7 次提取。对于病毒RNA 提取试 剂盒,包括了22 个带有相同的 SARS-CoV-2 和 SNM 模板的样 本。每个 OT-2 运行中都包括1个阴性对照样本(nuclease-free H2O) 。OT-2 的设备装配了 GEN2 磁珠纯化模块、p300 多通道 移液器和可选配的 GEN2 温控模块,对于 RNA 实验来说,为保证 更好的实验效果,建议配备温控模块。根据不同的试剂盒,需要 使用大概14盒300 μL 吸头,1 个 NEST 的单孔储液器,1 个NEST 2 mL深孔板,2个 NEST12 孔储液槽和1个PCR 孔板。
引物:疾病控制与预防中心(CDC)的引物和探针:
2019-nCoV_N1-F(GACCCCAAAATCAGCGAAAT)
2019-nCoV_N1-R (TCTGGTTACTGCCAGTTGAATCTG)
2019-nCoV_N1-P(FAM-
ACCCCGCATTACGTTTGGTGGACC-BHQ1)
2019-nCoV_N2-F(TTACAAACATTGGCCGCAAA)
2019-nCoV_N2-R(GCGCGACATTCCGAAGAA)
2019-nCoV_N2-P(FAMACAATTTGCCCCCAGCGCTTCAG-BHQ1)
RP-F(AGATTTGGACCTGCGAGCG),
RP-R(GAGCGGCTGTCTCCACAAGT)
RP-P (FAM-TTCTGACCTGAAGGCTCTGCGCG-BHQ1)
CDC 引物和探针订购自从Integrated DNA Technologies公司,又名IDT (2019-nCoV CDC EUA试剂盒)。N1、N2 和RNase P以CDC 推荐的浓度进行预混。
16s 引物:
Forward (CCTATAAGACTGGGATAACTTCGGG)
Reverse (CTTTGAGTTTCAACCTTGCGGTCG)
16s 引物从IDT 订购,于IDTE 1XTE 溶液 pH:8.0(DT) 中重悬,稀释至10uM 的工作浓度。
定量测量: DNA 和 RNA 样本的浓度可以使用 Qubit 4.0 FluorometerM(Thermo Fisher)进行定量测量。
此外,所有样品均在 PCR max ECO48 实时 PCR 系统上进行 qPCR 定 量。RNA 样品使用Luna°通用探针一步式 RT-qPCR 试剂盒(NEB) 进行 测试,浓度由 Lista 、Maria Jose 等人测试(3)。 进行以下程序:在 55℃下进行逆转录10分钟。初始变性在95℃下进行1 分钟,然后进 行50个循环,即在95℃下变性10秒,并在60℃下退火30秒。使用 Luna Universal qPCR Master Mix (NEB)以制造商推荐的浓度对DNA样 品进行测试。使用以下程序:初始变性在95℃下进行60秒,随后变性和延伸分别在95℃和60℃下进行15秒和30秒,持续40个循环。
实验结果
通过 qPCR 和荧光计分析测量, OT-2 提取的核酸数量接 近,核酸样品的 一 致性更高。
OT-2 经过了符合EUA 标 准 的性能测试,可以与多种qPCR 核提取试剂盒 一 起使用。
使用九种常用的提取试剂盒处理人类唾液和植物乳杆菌细菌培养 物,并使用两种常见的 qPCR 靶标进行 qPCR 分析: RNase P 用于 唾液样本,16s 用于细菌样本。使用六个试剂盒处理大肠杆菌培养物并使用荧光分析进行分析。
产量通过qPCR 中的循环阈值(Ct) 和荧光计中所得的ng/μL进行评估。 一致性则通过Ct值的变异系数 (CV) 进行评估。
Ct值反映了样品跨过高于背景信号的阈值所需的复制周期量,因此 它们传达了数量的倒数测量。对于这些目标,在此类样品中,25-35的 Ct 值较为可靠。
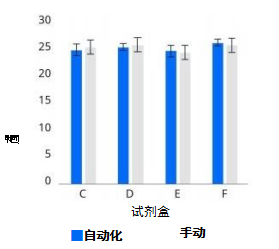
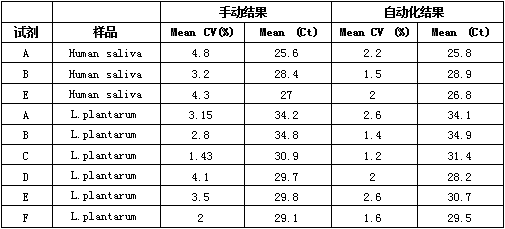
通过所有提取试剂盒进行检验测试,使用OT-2自动化系统进行核酸 提取纯化可以得到具有较低CV 和可比产量的Ct值(见图1和表2)。熟练的技术人员和OT-2返回的平均Ct值为25-35。
手动处理的CV 值为1.41-4.8, OT-2 的CV 值为1.2-2.6。熟练的技术 人员和OT-2提供了可比且一致的24-26 ng/μL的产量。这些结果表明, OT-2能够在提高一致性和重复性的同时提供高产量。
在与新冠病毒相关的测试中,使用合成的 SARS-CoV-2 样本和七种 常用的提取试剂盒进行了qPCR。 我们使用了 SNM 中的人类基因组 DNA 作为内部对照,使用CDC 的 SARS-CoV-2N1 和 N2 引物进行定量分析,同时使用 CDC 的 RP 引物作为阳性对照。
这项测试旨在评估使用不同提取试剂盒在 OT-2 上进行新冠病毒 qPCR 分析的性能。通过使用合成的 SARS-CoV-2 样本以及内部对 照和阳性对照,可以判断 OT-2 在检测病毒基因组的准确性和可靠性。
对qPCR 性能的评估是基于 PCR 检测紧急使用授权 (EUA) 标准。 为了满足 EUA 标准, 一个测试必须达到95%的扩增效果,也就是说,在qPCR 中,95%的样本必须产生可检测的N1和N2信号。
在这种性能评估中,我们还对 qPCR Ct 值进行了评估。对于这些目标,在这类样本中,标准 Ct值应该在30-40之间。
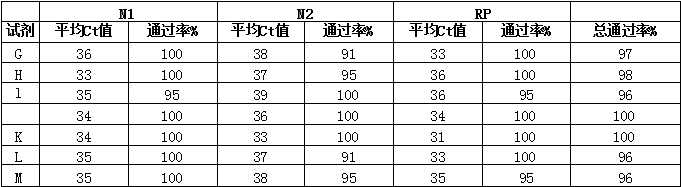
根据表格 3 的结果,OT-2 几乎在所有试剂盒上的表现均通过了 EUA 标准。除了两个由于裂解缓冲液过分粘稠导致妨碍了提取过程 的试剂盒只有91%的测试结果合格。并且,所有被测试的试剂中, 样品结果均实现了31-39的标准 Ct 值。这些结果表明,OT-2 系统可以与各种品牌的试剂配套使用,并达到临床标准。
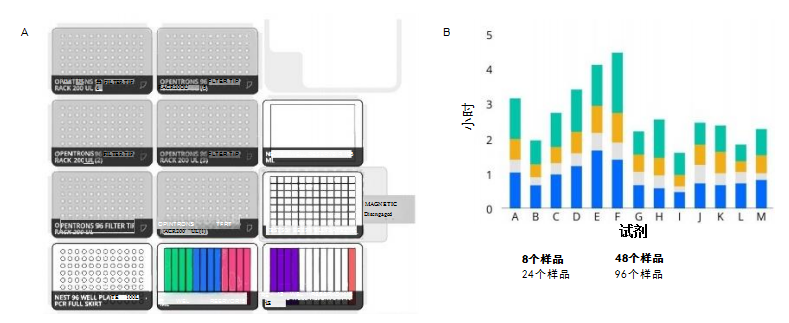
为了测试OT-2 系统的吞吐量和速度,我们使用了13种热门试剂盒 进行了RNA 和DNA 提取,并覆盖了不同长度。为了全面评估不同吞 吐量下的速度,测试了每批8、24、48和96个样本的情况。以从原始样品到纯化核酸所需的时间来衡量实验结果。
在这些提取试剂方案中,OT-2 系统在各种试剂盒和长度下实现了 快速提取的结果。在最短的协议中,处理8 个样本只需要25 分 钟,在最长的协议中,处理96个样本不到5小时(图2)。对于8 个样本的处理时长, OT-2 在13种试剂盒中平均处理时间为52分 钟。而在96个样本的情况下, OT-2 在13种试剂盒中平均处理时间 为2小时45分钟。这些结果表明, OT-2系统可以将其高性能与高吞吐量相结合,显著改善提取工作流程。
研究思考
OT-2 核酸提取工作站从有机和合成原始模板中提供了优质的 RNA 和 DNA 样品。通过 qPCR 和荧光测试发现,该自动化系统产生的 产出与由高技术水平操作人员执行的手动结果相当,并且在实验复 现率和精确性方面超过了手动操作的性能。研究表明,OT-2 成功 地达到了满足紧急使用授权 (EUA) 标准级别性能的要求, qPCR 信号检测的成功率超过了95%。时间测试显示,OT-2 处理8个样 品的时间不到1小时,对于96个样品的处理时间不到3 小时,这 是针对具有不同协议长度的试剂盒的平均值。事实上,使用最快的 试剂盒,OT-2 处理8个样品只需要25分钟,处理96个样品仅需1个半小时。
应用总结
●对于中等通量的实验室来说,光是节省的时间就足以让OT-2
在不到6个月的时间内回本。
●OT-2每次处理24个样品的提取可节省3.5小时的人工操作时 间。与手动操作相比,更高的吞吐量带来更好的精确性、减少
的变异性和提高的可重复性。
●这种高性能可以促进更好的质量控制,减少下游数据的变异 性。此外,消除了繁琐的人工操作程序可以减少错误,并降低
因为使用昂贵试剂重复运行程序而产生的成本。
这些测试都是在具有临床和实验室意义的多个样品以及各种不同的提取试剂盒中进行的。OT-2 的灵活性使其能够适应各种协议、试剂和样本类型,以持续提供优质的结果。
经验丰富的服务团队和强大的生产支持团队为客户提供无忧的订单服务。

简体中文

繁體中文

English

日本語

한국인