-
应用笔记 · 2025年08月12日
应用笔记 | Opentrons Flex 驱动的全自动化样本制备,助力 TMT 标记多重 LC-MS 蛋白质组学分析
阅读全文 -
应用笔记 · 2025年07月14日
应用笔记 | 基于 Opentrons Flex 的自动化蛋白质酶解与纯化
阅读全文 -
应用笔记 · 2025年07月07日
应用笔记 | 基于 Opentrons Flex 的自动化蛋白质浓度定量与均一化处理
阅读全文


在单克隆抗体(mAb)制备领域,相较于传统的杂交瘤技术,基因工程表达载体在复制具有长期稳定性的分子级抗体方面展现出更高效的优势。特别是在研发的早期阶段,能够自动化生产用于临床前研究的治疗性 mAb 候选物(例如,具有修饰可变区的全长 IgG),已引起研发人员的极大兴趣。
基于以上背景,Opentrons 应用科学家 Boren Lin 博士和 Kinnari Watson 博士,测试并验证了 Opentrons 自动化移液工作站 OT-2 和 Flex 在这一流程中的应用。
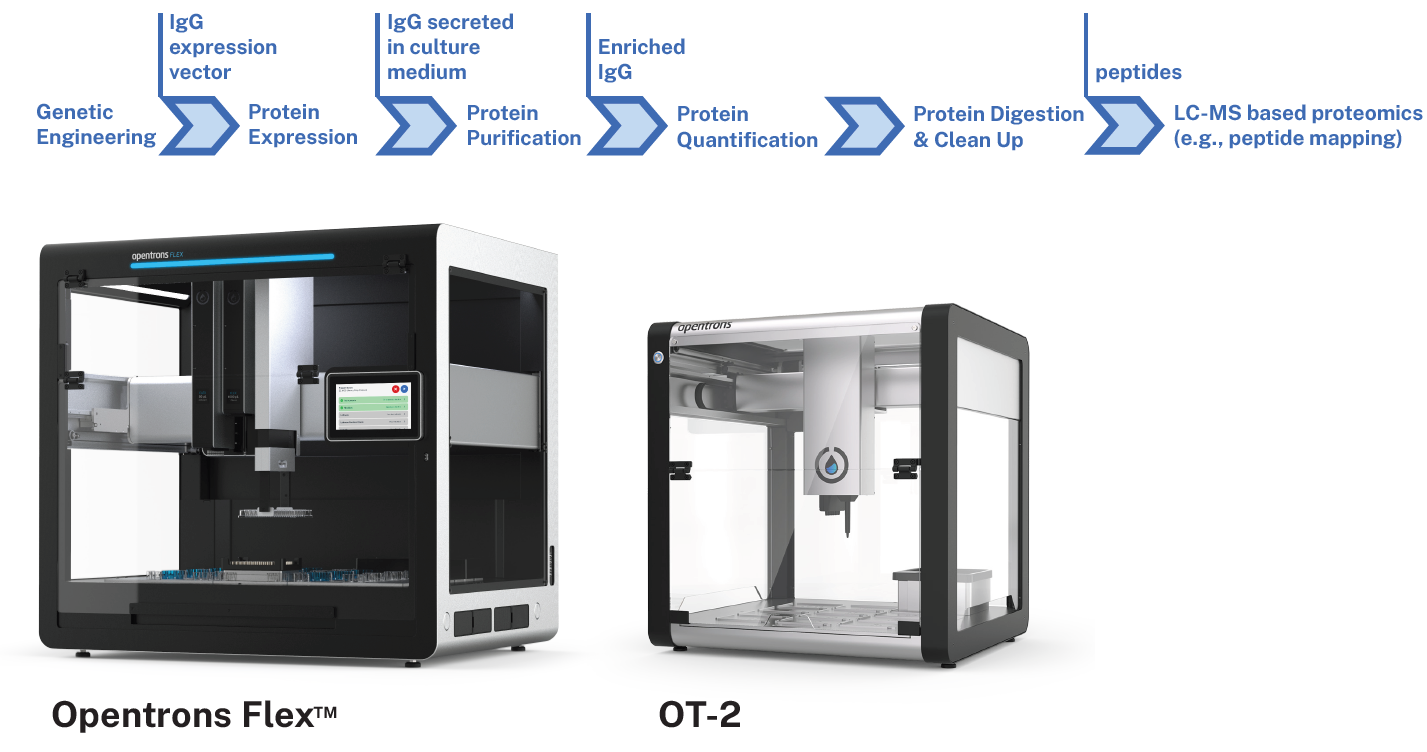
方法
蛋白表达流程
平台:Opentrons OT-2(配备 HEPA 模块)
工作流程
第 1 天:在 6 孔板中准备 HeLa 细胞(37°C 和 5% CO2,悬浮培养)
第 2 天:准备 DNA /转染试剂混合物(Thermo Scientific, Waltham, MA 的 pRABBIT IgG IRES-EmGFP 阳性对照载体,和 Promega, Madison, WI 的 FuGENE HD 转染试剂),并将上述混合物加入 HeLa 细胞培养物中(37°C 和 5% CO2,悬浮培养)
第 5 天:收集培养基(将收集的产物进行蛋白纯化)
蛋白纯化流程
平台:Opentrons Flex(配备加热振荡模块和磁力模块)
工作流程
1. 用平衡缓冲液对Dynabeads Protein G(Thermo Scientific, Waltham, MA)进行预处理
2. 孵育并混匀样品/磁珠混合物以捕获目标蛋白(持续混匀 2 小时)
3. 洗涤 2 次
4. 洗脱目标蛋白
最终产物进行 SDS-PAGE、Western Blot 和蛋白定量检测
蛋白定量检测流程
平台:Opentrons Flex(配备温控模块)
工作流程
1. 准备工作试剂(Thermo Scientific, Waltham, MA 的 BCA 蛋白测定试剂)
2. 将工作试剂、样品和标准品加入 96 孔板中用以准备工作板
3. 孵育(37°C,30 分钟)
通过在平台外的读数器上测量 560 nm 的吸光度获得读数,并通过参照标准曲线估算蛋白水平。
蛋白消化和纯化流程
平台:Opentrons Flex(配备热循环模块)
工作流程
1. 还原:在37°C下使用DTT处理30分钟
2. 烷基化:在室温下使用IAA处理30分钟
3. 消化:在37°C下使用胰蛋白酶处理16小时
4. 纯化:使用SP3方法对消化后的样品进行脱盐处理,该过程采用Sera-Mag SpeedBead羧基化修饰磁珠(Cytiva,Marlborough, MA)
5. 收集洗脱液并进行真空干燥(平台外操作)
最终产品进行液相色谱-质谱(LC-MS)分析。
流程脚本在开放源代码的 Opentrons Protocol 协议库中提供:
细胞培养准备(最多 4 块板)
DNA 转染(最多 4 块板)
用于免疫沉淀的 Dynabeads
用于免疫沉淀的 Dynabeads---15 mL 试管中的试剂
BCA 蛋白测定
结果
通过 OT-2 平台上的自动化蛋白表达流程转染载有 IgG cDNA 的 HeLa 细胞,并通过荧光显微镜观察到 GFP 表达确认转染成功 (图 1)。
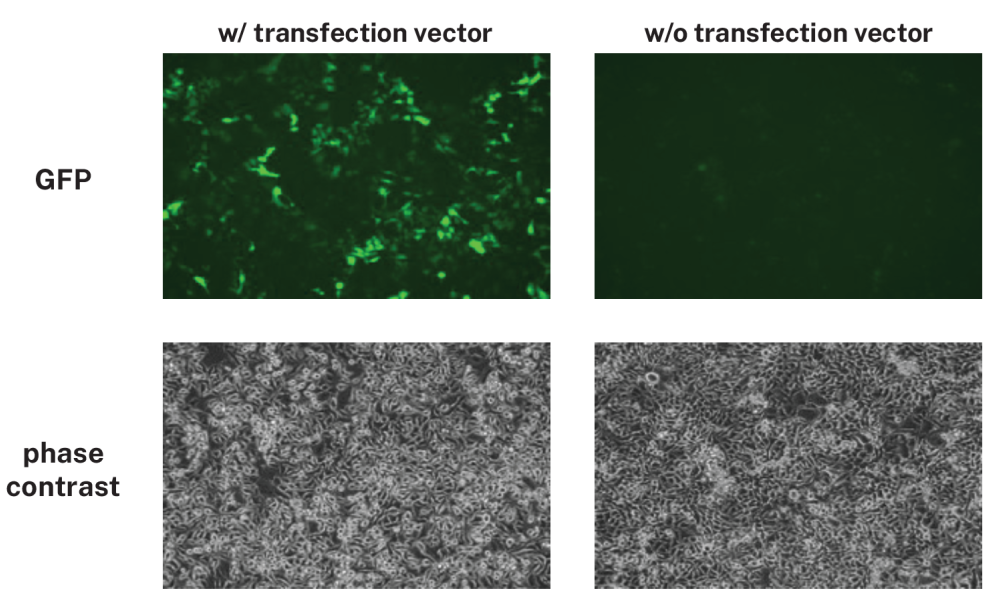
图 1:HeLa 细胞在 6 孔板中以 70% 汇合度接种,然后培养过夜。每孔的转染 Master Mix 通过将 DNA(2 μg)与 FuGene 转染试剂(6 μL)混合在无血清的 DMEM(100 μL)中制备。室温孵育 10 分钟后,在配备 HEPA 模块的 OT-2 上运行蛋白表达流程。转染的细胞培养 72 小时,并使用 EVOS M7000(Thermo Scientific,Waltham,MA)拍摄图像,并收获培养基。
通过 Flex 平台上的自动化蛋白纯化流程处理从转染的 HeLa 细胞培养物中收获的上清液以收集分泌的 IgG,并通过 SDS-PAGE 和 Western Blot 确认纯化的 IgG (图 2)。
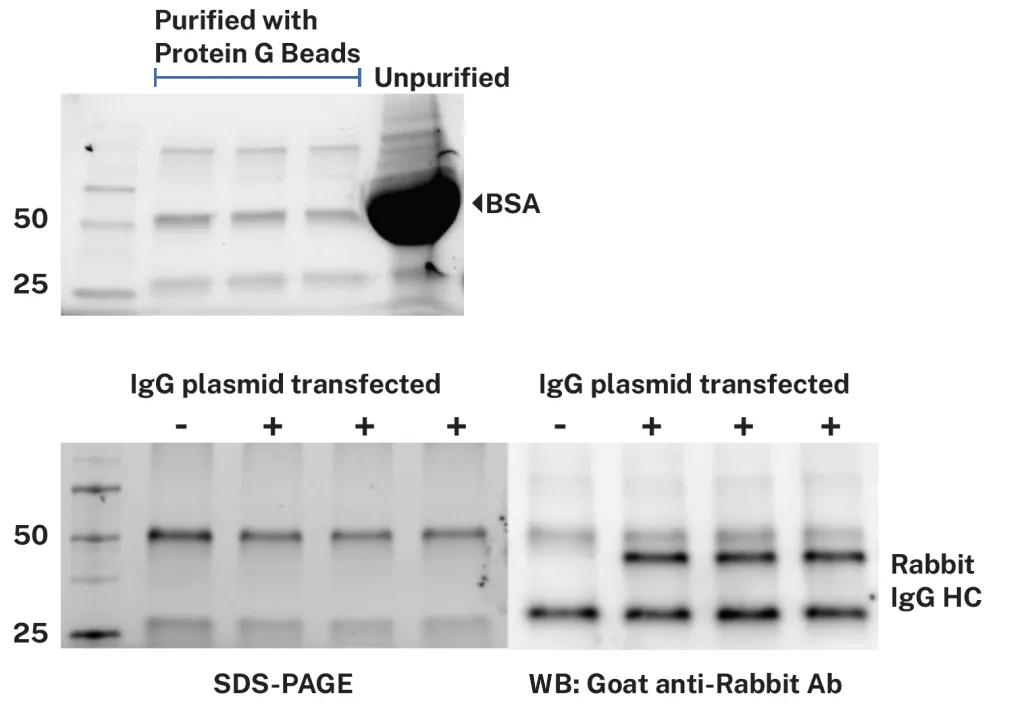
图 2:转染 72 小时后收集的培养基在 Flex 上使用 Dynabeads Protein G 进行 IgG 分离,并将洗脱产物进行 SDS-PAGE 和 Western Blot 分析。上图:纯化与未纯化培养基;下图:使用IRDye® 680RD Goat anti-Rabbit IgG (LI-COR Biosciences,Lincoln,NE) 检测到的兔 IgG。
通过 Flex 平台上的自动化蛋白定量流程对最终产物中纯化后的 IgG 进行 BCA 蛋白检测 (图 3)。
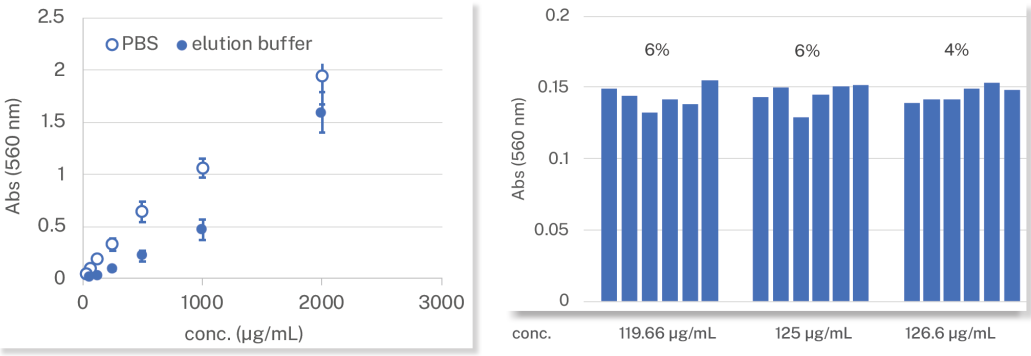
图 3:使用 PBS 或者其他用于蛋白纯化后洗脱的缓冲液,对 BSA(起始浓度: 200 ug/mL)进行 2 倍梯度稀释,各个梯度取 25 ul 进行 BCA 测定。用读扳机测定吸光度后绘制标准曲线。基于 n = 4 获得的均值和标准偏差(左图)。通过蛋白纯化流程收集的洗脱产物进行了 BCA 蛋白测定,并估算蛋白浓度。基于 n = 6 获得的均值和变异系数(右图)。
通过蛋白消化和纯化流程处理的样品显示良好的基峰离子色谱图。所有肽样品中均检测到兔 IgG (图 4)
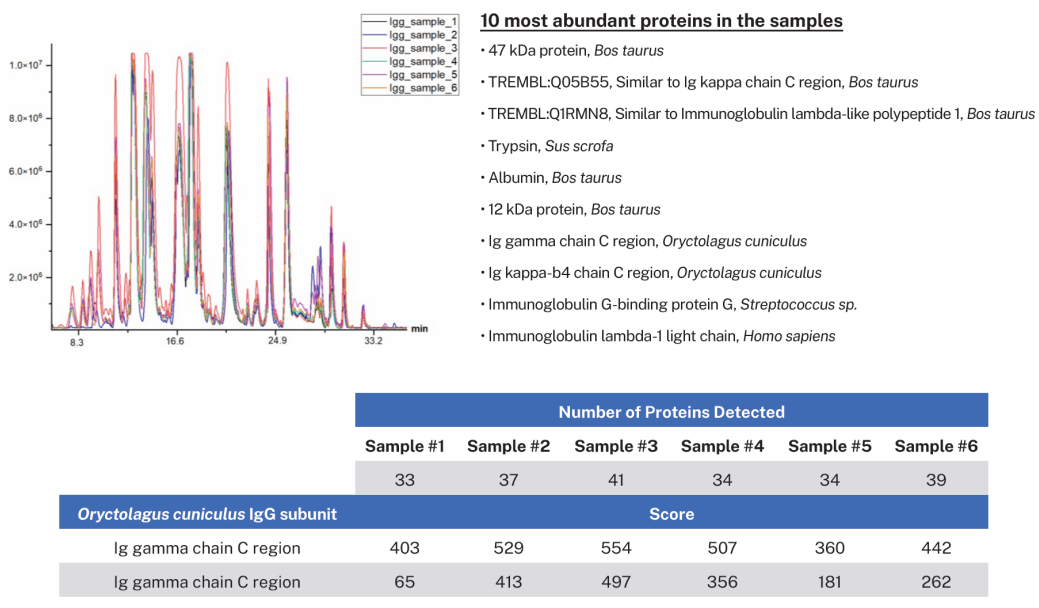
图 4:已纯化的 6 个兔 IgG 样品在纽约市立大学高级科学研究中心(纽约,NY)通过 Bruker’s maXis-II ETD ESI-QqTOF/Dionex Ultimate-3000 液相色谱系统进行分析。(上图)基峰强度色谱图(离子电流 vs. 保留时间)和(下图)检测到的蛋白质。
结论
在本研究中,我们成功利用 Opentrons 自动化移液工作站,通过一系列自动化策略优化了重组单克隆抗体(mAb)生产的关键环节, 包括蛋白质的表达、纯化、定量分析以及蛋白质组学样品的制备。初步实验结果不仅验证了自动化流程的可行性,还显著减少了手动操作时间,并展示了其在高通量样品制备方面的潜力。
经验丰富的服务团队和强大的生产支持团队为客户提供无忧的订单服务。

简体中文

繁體中文

English

日本語

한국인